国际石油价格多次上涨,为解决能源危机,现在全面推广使用乙醇汽油作为发动机燃料,即在汽油中掺入一定比例的乙醇,以代替一部分汽油.已知热化学方程式: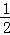 C2H5OH(l)+
C2H5OH(l)+ O2(g)=CO2(g)+
O2(g)=CO2(g)+ H2O(l)△H=﹣683.4kJ/mol.下列有关说法正确的是
H2O(l)△H=﹣683.4kJ/mol.下列有关说法正确的是
| A.乙醇汽油是一种清洁能源,燃烧不会产生任何污染 |
| B.在25℃、101KPa时,生成1mol水时放出683.4kJ的热量 |
| C.乙醇的燃烧热为683.4kJ/mol |
| D.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=﹣1366.8kJ/mol |
短周期元素形成的纯净物A、B、C、D、E,五种物质之间的转化关系如图1所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的一种相同).
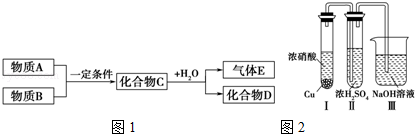
请回答下列问题:
(1)若C是离子化合物,D是一种强碱,则C的化学式 ,并任写一种C的主要用途 .
(2)若E的水溶液呈弱酸性,D是既能溶于强酸、又能溶于强碱的化合物.
①用电离方程式解释D既能溶于强酸、又能溶于强碱的原因(仅写出电离方程式即可): .
②用电荷守恒的等式表示E与NaOH溶液反应生成正盐的溶液中所有离子的浓度之间的关系: .
(3)若C是一种气体,D是一种强酸,则:
①C与水反应的化学方程式为 .
②已知常温下物质A与物质B反应生成1mol气体C的△H=﹣57kJ•mol﹣1,1mol气体C与H2O反应生成化合物D和气体E的△H=﹣46kJ•mol﹣1,写出物质A与物质B及水反应生成化合物D的热化学方程式为 .
③有人认为“浓H2SO4可以干燥气体C”.某同学为了验证该观点是否正确,用如图2所示装置进行实验.
实验过程中,在浓H2SO4中未发现有气体逸出,则得出的结论是 .
④用铂做电极电解H2SO4的溶液,其阳极的电极反应式为 .
研究性学习小组进行了一系列化学实验后,发现高锰酸钾分解后的含锰元素的化合物都能和浓盐酸反应制得氯气,且锰化合物的还原产物都是MnCl2.他们将6.32gKMnO4粉末加热一段时间,也不知道高锰酸钾是否完全分解,收集到0.112L气体后便停止加热了,冷却后放入足量的浓盐酸再加热,又收集到气体体积是(上述气体体积都折合成标准状况)
| A.0.448L | B.2.240L | C.2.016L | D.无法确定 |
下列说法错误的是
①NaHCO3溶液加水稀释, 的比值保持增大
的比值保持增大
②浓度均为0.1mol•L﹣1的Na2CO3、NaHCO3混合溶液:2c(Na+)═3[c(CO32﹣)+c(HCO3﹣)]
③在0.1mol•L﹣1氨水中滴加0.lmol•L﹣1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH﹣)=l0﹣amol•L﹣1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32﹣)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH﹣)+c(H2S)+c(HS)
| A.①④ | B.②⑤ | C.①③ | D.②④ |
24mL浓度为0.05mol・L﹣1的Na2SO3溶液,恰好与20mL浓度为0.02mol・L﹣1的K2Cr2O7溶液完全反应,已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
| A.+2 | B.+3 | C.+4 | D.+5 |
近来,制备和利用氢气这一清洁能源已有多项成果。
(1)德国克莱斯公司成功研制了甲醇(CH3OH)制氢车载燃料电池工艺,其原理如下流程图所示:

①流程图中,甲醇与水在选择氧化器中反应生成二氧化碳和氢气,写出该反应的化学方程式
②该车载燃料电池的介质为碱性环境,请写出该燃料电池的正极反应式为
(2)美国Bay等工厂成功研制了以甲烷来制取氢气,其生产流程如下图:

①此流程的第Ⅱ步反应为:CO(g)+H2O(g) H2(g)+CO2(g),该反应的化学平衡常数表达式K=
H2(g)+CO2(g),该反应的化学平衡常数表达式K=
②此流程的第Ⅱ步反应的平衡常数随温度的变化如下表,在830 ℃、以表中的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有________(填实验编号)。
| 温度/℃ |
400 |
500 |
830 |
1 000 |
| 平衡常数K |
10 |
9 |
1 |
0.6 |
| 实验编号 |
n(CO) |
n(H2O) |
n(H2) |
n(CO2) |
| A |
1 |
5 |
2 |
3 |
| B |
2 |
2 |
1 |
1 |
| C |
3 |
3 |
0 |
0 |
| D |
0.5 |
2 |
1 |
1 |
③若400 ℃时,第Ⅱ步反应生成1 mol氢气的热效应值为33.2kJ,第Ⅰ步反应的热化学方程式为:CH4(g) + H2O(g) === 3H2(g) + CO(g) ΔH=-103.3 kJ·mol-1则400 ℃时,甲烷和水蒸反应生成二氧化碳和氢气的热化学方程式为:
(3)我国科学家研究了常温下利用Pt等催化剂在可见光作用下使水分解制氢气的方法,下图是三种催化剂在光照分解水实验中的效果比较图。

要得出如图所示的实验结果,需要测定的实验数据是 ,本实验的目的是 。
(1) 图中A为直流电源,B为浸透饱和氯化钠和酚酞溶液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色。
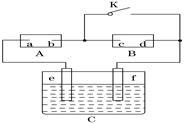
①电源A中a点为________极。
②滤纸B上发生的总反应的离子方程式为 。
③欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为 ,电镀槽中盛放的电镀液可以是________或________。
(2)加碘盐中的KIO3也可以用电化学氧化法制取:电解KI溶液可以制取KIO3。则电解时阳极材料可选用 (填“石墨”或“铜”)。写出该电极反应方程式
下列有关电解质溶液的推理,其中不正确的是( )
| A.室温下,pH=4的CH3COOH溶液和pH=10的NaOH溶液等体积混合, 所得溶液pH<7 |
| B.用蒸馏水稀释0.1mol/L CH3COOH溶液至0.01mol/L,若稀释过程温度不变,则稀释过程中c(H+) / c(CH3COOH)呈增大的趋势 |
| C.将0.2mol/L的弱酸HX溶液与0.1mol/L的NaOH溶液等体积混合,充分反应后,溶液中存在:2c(OH-) +c(X-)=2c(H+) + c(HX) |
| D.用0.2mol/L的NaOH标准溶液滴定HCl与CH3COOH的混合溶液,当中和至中性时,溶液中存在:c(Na+)+c(CH3COOH) = c(Cl-) + c(CH3COO-) |
下列相关实验能达到预期目的的是( )
| |
相关实验 |
预期目的 |
| A |
相同温度下,将等质量的大理石块、大理石粉末分别加入等体积、等浓度的盐酸和醋酸中,观察气泡产生的快慢 |
验证固体接触面积对化学反应速率的影响 |
| B |
可逆反应FeCl3(aq)+3KSCN(aq) Fe(SCN)3(aq)+3KCl(aq)建立平衡后,在其它条件不变时,加入KCl固体,观察体系颜色的变化 Fe(SCN)3(aq)+3KCl(aq)建立平衡后,在其它条件不变时,加入KCl固体,观察体系颜色的变化 |
验证浓度对化学平衡的影响 |
| C |
室温下,向BaSO4悬浊液中加入饱和Na2CO3溶液,过滤后,再向沉淀中加入盐酸,沉淀部分溶解 |
验证BaSO4和BaCO3Ksp的相对大小 |
| D |
相同温度下,两支试管中装有等体积、等浓度的H2O2溶液,向其中分别加入少量FeCl3固体和少量的MnO2固体 |
验证不同催化剂对H2O2分解速率的影响 |
下列有关化学实验事实描述正确的是( )
A.Na2CO3溶液呈碱性的原因是:CO32-+2H2O H2CO3+2OH- H2CO3+2OH- |
| B.用NaAlO2溶液可以鉴别Na2CO3溶液和NaHCO3溶液 |
| C.有NH4+浓度相等的NH4Cl、CH3COONH4和NH4Al(SO4)2三种溶液,测得相同温度下溶质浓度最大的是NH4Al(SO4)2溶液 |
| D.AlCl3溶液和NaAlO2溶液加热蒸干所得主要成分都是Al(OH)3固体 |
按图甲装置进行实验,若图乙中横坐标x表示通过电极的电子的物质的量,下列叙述正确的是 ( )
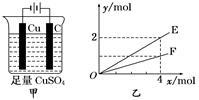
| A.电解过程中,Cu2+浓度不变 |
| B.E表示反应生成O2的物质的量 |
| C.电解过程中,石墨棒附近溶液的pH有所增大 |
| D.若向烧杯中加入2 mol CuO可以使电解质恢复到电解前的浓度,则电解过程中共转移了4mol电子。 |
已知分子式为C12H12的物质A的结构简式为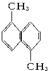 ,其苯环上的二溴代物有9种同分异构体,由此推断A苯环上的四溴代物的同分异构体的数目有( )
,其苯环上的二溴代物有9种同分异构体,由此推断A苯环上的四溴代物的同分异构体的数目有( )
| A.9种 | B.10种 | C.11种 | D.12种 |
用a、b两个质量相等的Pt电极电解AlCl3和CuSO4的混合溶液[ n(AlCl3) : n(CuSO4) = 1:9 ]。 t1时刻a电极得到混合气体,其中Cl2在标准状况下为224 mL(忽略气体的溶解);t2时刻Cu全部在电极上析出。下列判断正确的是
| A.a电极与电源的负极相连 |
| B.t2时,两电极的质量相差3.84g |
| C.电解过程中,溶液的pH不断增大 |
| D.t2时,b的电极反应是4OH――4e-=2H2O+O2↑ |
甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成.电池的总反应式为2CH3OH+3O2+4OH-═2CO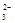 +6H2O.则下列说法正确的是
+6H2O.则下列说法正确的是
| A.电池放电时通入空气的电极为负极 |
| B.电池放电时负极的电极反应式为CH3OH-6e-+H2O═CO2↑+6H+ |
C.由于CO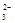 水解显碱性,电池放电时,电解质溶液的pH逐渐增大 水解显碱性,电池放电时,电解质溶液的pH逐渐增大 |
| D.电池放电时每消耗1molCH3OH转移6mol电子 |
常温时,Ksp[Mg(OH)2] = 1.1×10-11,Ksp(AgCl) = 1.8×10-10,Ksp(Ag2CrO4) = 1.9×10-12 Ksp(CH3COOAg) = 2.3×10-3,下列叙述不正确的是
| A.浓度均为0.2mol·L-1AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀 |
| B.将0.001mol·L-1的AgNO3溶液滴入0.001mol·L-1的KCl和0.001mol·L-1的K2CrO4的混合溶液中,先产生Ag2CrO4沉淀 |
| C.c(Mg2+)为0.11mol·L-1的溶液中要产生Mg(OH)2沉淀,溶液的pH要控制在9以上 |
| D.在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变 |
试题篮
()