利用周期表中同族元素的相似性,可预测元素的性质。
(1)P元素的基态原子有_______个未成对电子,白磷的分子式为P4,其结构如下图所示。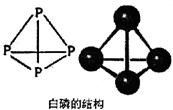
科学家目前合成了N4分子,N原子的杂化轨道类型是________,N -N键的键角为________;N4分解后能产生N2并释放出大量能量,推测其用途为________。
(2) N、P、As原子的第一电离能由大到小的顺序为________。
(3)立方氮化硼晶体的结构如下图所示:
该晶体中,B原子填充在N原子的________空隙,且占据此类空隙的比例为________ (填百分数)。
(4) N与As是同族元素,B与Ga是同族元素,立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是________;立方砷化镓晶体的晶胞边长为a pm,则其密度为________g·cm-3 (用含a的式子表示,设NA为阿伏加德罗常数的值)。
钴(Co)是人体必需的微量元素。含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用。请回答下列问题:
(1)Co基态原子的电子排布式为 ;
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学疗法中的光敏剂、催化剂等方面得到了广泛的应用。其结构如图所示,中心离子为钴离子。
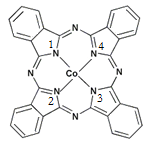
①酞菁钴中三种非金属原子的电负性由大到小的顺序为 ;
(用相应的元素符号作答);碳原子的杂化轨道类型为 ;
②与钴离子通过配位键结合的氮原子的编号是 ;
(3)CoCl2中结晶水数目不同呈现不同的颜色。
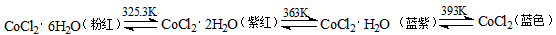
CoCl2可添加到硅胶(一种干燥剂,烘干后可再生反复使用)中制成变色硅胶。简述硅胶中添加CoCl2的作用: ;
(4)用KCN处理含Co2+的盐溶液,有红色的Co(CN)2析出,将它溶于过 量的KCN溶液后,可生成紫色的[Co(CN)6]4-,该配离子具有强还原性,在加热时能与水反应生成淡黄色[Co(CN)6]3-,写出该反应的离子方程式: ;
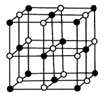
(5)Co的一种氧化物的晶胞如右图所示,在该晶体中与一个钴原子等距离且最近的钴原子有________个;筑波材料科学国家实验室一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是 。
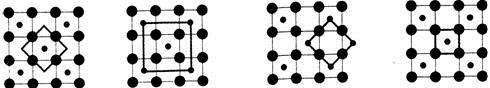
A. B. C. D.
1905年德国化学家哈伯发明了合成氨的方法,他因此获得了1918年度诺贝尔化学奖。氨的合成不仅解决了地球上因粮食不足而导致的饥饿与死亡问题,在国防、能源、轻工业方面也有广泛用途。
Ⅰ.以氨为原料,合成尿素的反应原理为:
2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) ΔH =" a" kJ/mol。
CO(NH2)2(l)+H2O(g) ΔH =" a" kJ/mol。
为研究平衡时CO2的转化率与反应物投料比(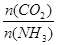 )及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应,并绘出下图(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。
)及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应,并绘出下图(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。
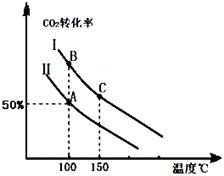
(1)a 0 (填“>”或“<”),判断依据是__________________。
(2)①投料比:Ⅰ Ⅱ(填“>”或“<”)。
②若n(CO2)起始="10" mol,曲线Ⅱ的投料比为0.4,在100℃条件下发生反应,达平衡至A点,则A点与起始压强比为_________________。
③A点平衡常数与B点平衡常数间的关系:KA KB (填“>”或“<”或“=”)。B点正反应速率与C点正反应速率间的关系为:v (B)_________v (C) (填“>”或“<”或“=”)。
(3)若按曲线Ⅰ的投料比投料,在上述实验中压缩容器体积至5L,在上图中画出反应达平衡时的二氧化碳的转化率与温度之间的关系曲线。
(4)为提高CO2转化率可以采取的措施是 。
a.使用催化剂
b.及时从体系中分离出部分CO(NH2)2
c.将体系中的水蒸气液化分离
Ⅱ.氨气可用于工业上生产硝酸,其尾气中的NO2可用氨水吸收生成硝酸铵,25℃时,将10molNH4NO3溶于水,溶液显酸性,向该溶液中滴加1L某浓度的氨水,溶液呈中性,则滴加氨水的过程中水的电离平衡将_________(填“正向”、“逆向”或“不”) 移动, 此中性溶液中NH3·H2O的物质的量为________mol。(25℃时,NH3·H2O的电离平衡常数Kb=2×10-5)
雾霾含有大量的污染物SO2、NO。工业上变废为宝利用工业尾气获得NH4NO3产品的流程图如下:(Ce为铈元素)

(1)上述流程中循环使用的物质有 。
(2)上述合成路线中用到15%~20%的乙醇胺(HOCH2CH2NH2),其水溶液具有弱碱性,显碱性的原因:HOCH2CH2NH2 + H2O HOCH2CH2NH3+ + OH-,写出乙醇胺吸收CO2的化学方程式__________。
HOCH2CH2NH3+ + OH-,写出乙醇胺吸收CO2的化学方程式__________。
(3)写出吸收池Ⅲ中,酸性条件下NO转化为NO2-的离子方程式为 。
(4)向吸收池Ⅳ得到的HSO3﹣溶液中滴加少量CaCl2溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因: 。
(5)电解池Ⅴ可使Ce4+再生,装置如下图所示:

生成Ce4+从__________口(填字母)流出,写出阴极的电极反应式 :
(6)从氧化池Ⅵ中得到粗产品NH4NO3的实验操作是 、 、过滤、洗涤等。上述流程中每一步均恰好完全反应,若制得NH4NO3质量为xkg,电解池V制得cmol/L的S2O32﹣溶液ym3,则氧化池Ⅵ中消耗的O2在标准状况下的体积为 m3。
(1)AlCl3溶液与NaOH溶液反应时,当Al3+的物质的量与OH-的物质的量之比(以下均填物质的量之比)为________时,Al(OH)3沉淀量最多。
(2)NaAlO2溶液与盐酸溶液反应时,AlO的物质的量与H+的物质的量之比为________时,Al(OH)3沉淀恰好溶解。
将V mL NO和NO2的混合气体通过足量的水,充分反应后,得到一定体积的无色气体A。将此无色气体A与等体积的氧气混合,充分反应后,再通过足量的水,充分反应后还能收集到5 mL无色气体(以上气体体积均在相同状况下测定)。试回答:
(1)A是 ,其体积为 mL。
(2)反应过程中涉及的化学方程式:
(1)常温下,0.1 mol/L的醋酸和0.1 mol/L的盐酸各100 mL,分别与足量的锌粒反应,产生的气体体积前者 后者(填“<”、“>”或“=”).
(2)将体积和物质的量浓度都相同的醋酸和氢氧化钠溶液混合后,溶液呈 性(填“酸”,“中”或“碱”下同),溶液中 c(Na+ ) c(CH3 COO- )(填“ >” 或“=”或“<”,下同 )。
(3)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 性,溶液中c(Na+) c(CH3COO- )
(4)用Al2(SO4)3 与NaHCO3 溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式___________。
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2 的含量及有效地开发利用CO2 ,引起了各国的普遍重视。
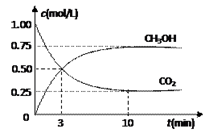
(1)目前工业上有一种方法是用CO2 来生产燃料甲醇。为探究反应原理,现进行如下实验,
在体积为1 L的密闭容器中,充入1mol CO2 和3mol H2 ,一定条件下发生反应:
CO2 (g)+3H2 (g) CH3OH(g)+H2O(g) △H=-49.0kJ/mol
CH3OH(g)+H2O(g) △H=-49.0kJ/mol
测得CO2 和CH3OH(g)的浓度随时间变化如图所示。
①从反应开始到平衡,氢气的平均反应速率 v (H2 )=___________mol/(L·min)。
②该反应的平衡常数表达式为__________________。
③下列措施中能使 n(CH3OH)/n(CO2)增大的是___________。
| A.升高温度 | B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离 | D.再充入1molCO2 和3molH2 |
(2)①在载人航天器的生态系统中,不仅要求分离去除CO2 ,还要求提供充足的O2 。某种电化学装置可实现如下转化:2CO2 =2CO+O2 ,CO可用作燃料。
已知该反应的阳极反应为:4OH— —4e— =O2↑+2H2O
则阴极反应式为:____________________________。
②有人提出,可以设计反应2CO=2C+O2 (△ H >0、△S<0)来消除CO的污染。请你判断是否可行并说出理由:_________;____________________________________。
课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:
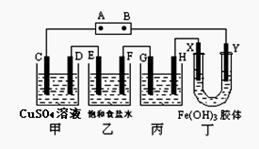
(1)电源A 极的名称是 (正极或负极)。
(2)甲装置中电解反应的总化学方程式是 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是 。
(4)欲用丙装置给铜镀银,G应该是 (填“铜”或“银”),电镀液的主要成分是 (填化学式)。
(5)装置丁中的现象是_____________________
硫及其化合物在国民生产中占有重要的地位。
(1)常温常压下,已知1g 硫完全燃烧放出a kJ的热量,写出硫燃烧热的热化学方程式
。
(2)又已知2H2S(g)+O2(g)=2S(s)+2H2O(l) △H=-bkJ/mol,写出H2S完全燃烧生成二氧化硫和水的热化学方程式 。
请按要求回答下列问题:
(1)非诺洛芬是治疗类风湿性关节炎的药物,其结构简式如图: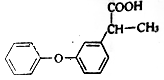
①非诺洛芬的含氧官能团名称为____________,②非诺洛芬能发生的有机反应类型有____________。
(2)写出下列反应的化学方程式:
①在加热、加压和催化剂条件下乙烯与水反应:______________________________。
②CH2=CHCOOCH2CH3的聚合反应:__________________________。
填空题
(1)碳原子最外电子层含有__________个电子,一个碳原子可以跟其他非金属原子形成__________共价键。
(2)在有机合成过程中,引入碳碳双键的三种方法是_____________、________________、_____________。
(3)根据官能团不同,单糖可分为_______________和________________________。
(4)核酸分为DNA和RNA,DNA的主要功能是________________;RNA的主要功能是____________。
钠和铝是两种重要的金属。请回答下列问题:
(1)一小块金属钠放置在空气中,观察到的现象是_________(填序号,下同);若金属钠长时间在潮湿的空气中放置,最后生成的物质是_________。
A.金属表面逐渐失去光泽 B.氢氧化钠 C.碳酸钠
(2)将一小块金属钠投入水中,观察到的实验现象是________(填序号),发生反应的离子方程式为:__________________。
A.钠沉到水底 B.钠熔成小球 C.小球四处游动
(3)铝与稀硝酸反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O,该反应的氧化剂是_______(填化学式),还原剂与氧化剂的物质的量之比是________,当有5.4gAl发生反应时,转移电子的物 质的量为________mol。
在工农业生产和日常生活中经常用到的物质有下列几种:①Si ②NH4Cl ③Ca(ClO)2 ④Al(OH)3 ⑤Fe2O3。其中:电脑芯片中常用的物质是__________(填序号,下同);用于杀菌、消毒的物质 是____________;用作化肥的是____________;用作红色油漆和涂料的是___________;医用胃酸中和剂的是 _____________。
Na2O2可作为潜水艇里氧气的来源。将3.9gNa2O2充分反应。
(1)Na2O2的物质的量为_________mol。
(2)生成的O2在标准状况下的体积为___________L。
(3)反应中转移的电子数为________(NA为阿伏加德罗常数的值)。
试题篮
()