碳酸二甲酯(DMC)是一种低毒性的绿色化学品,可用于代替高毒性的光气(COCl2)作羰基化试剂。DMC的合成路线如下图。完成下列填空。
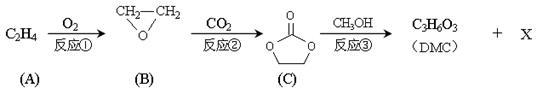
已知: RCO-OR1 + R2O-H→RCO-OR2 + R1O-H (称酯交换反应)
(1)写出反应类型:反应①________ ;反应③ _________ ;
(2)写出结构简式:DMC__________;X___________;
(3)已知物质Y与DMC互为同分异构体,Y的水溶液呈酸性,在一定条件下2 molY能生成1mol分子中含六元环结构的有机物Z,则Y的结构简式为________,Z的结构简式为________;
(4)DMC与双酚( )在一定条件下可发生类似反应①的反应,生成芳香族聚碳酸酯,写出反应的化学方程式:_______________________。
)在一定条件下可发生类似反应①的反应,生成芳香族聚碳酸酯,写出反应的化学方程式:_______________________。
2014年4月,英国《每日邮报》报道制造太阳镜、婴儿奶瓶、太空杯和光盘的主要材料都是聚碳酸酯,聚碳酸酯在一定条件下可释放出有毒的双酚A(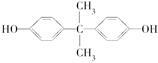 )。聚碳酸酯不耐高温,100 ℃时释放出的双酚A是25 ℃时的50倍。双酚A进入人体后,会溶解在身体的血管里,导致致命性的血管疾病。请回答下列问题:
)。聚碳酸酯不耐高温,100 ℃时释放出的双酚A是25 ℃时的50倍。双酚A进入人体后,会溶解在身体的血管里,导致致命性的血管疾病。请回答下列问题:
Ⅰ.下列关于双酚A的说法不正确的是________(填序号)
A.利用聚碳酸酯制成的茶杯来泡茶时对人体无害
B.双酚A的分子式是C15H16O2
C.双酚A的核磁共振氢谱显示有4组峰,且峰面积之比为1∶2∶2∶3
D.1 mol双酚A最多消耗2 mol Br2
Ⅱ.聚碳酸酯(简称PC)是分子链中含有碳酸酯基的高分子聚合物,其合成流程如下: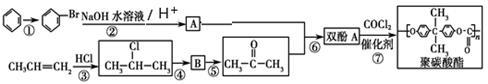
(1)反应①②③④⑤中属于取代反应的有________。
(2)CH3CH==CH2与Cl2加成产物的同分异构体有________种(不含加成产物)。
(3)写出反应⑤⑦的化学方程式:
反应⑤________________________。反应⑦________________________。
G(异戊酸薄荷醇酯)是一种治疗心脏病的药物,其合成路线如下: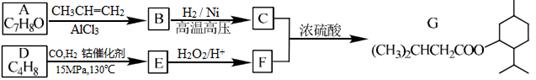
已知:
①A能与FeCl3溶液发生显色反应
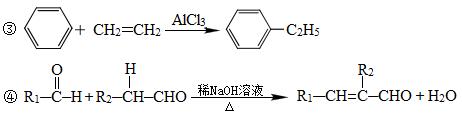
(1)A的结构简式为____________。
(2)C烃基上的一氯代物有种(不考虑立体异构)____________。
(3)D分子中含有种不同化学环境的氢原子____________。
(4)写出同时符合下列条件的A的所有同分异构体的结构简式(不考虑立体异构):____________。
a.分子中有6个碳原子在一条直线上
b.分子中含一个—OH
(5)正戊醇可用作香料、橡胶促进剂等,写出以乙醇为原料制备CH3(CH2)3CHO的合成路线流程图(无机试剂任用)。合成路线流程示意图示例如下:
A(C2H2)是基本有机化工原料。由A制备聚乙烯醇缩丁醛和顺式异戊二烯的合成路线(部分反应条件略去)如下所示: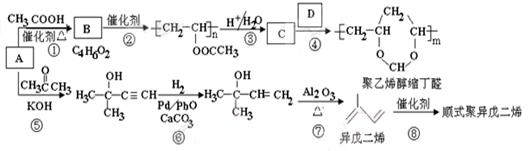
回答下列问题:
(1)A的名称是,B含有的官能团是_________。
(2)①的反应类型是_________,⑦的反应类型是_________。
(3)C和D的结构简式分别为____________、____________。
(4)异戊二烯分子中最多有个原子共平面,顺式聚异戊二烯的结构简式为____________。
(5)写出与A具有相同官能团的异戊二烯的所有同分异构体(填结构简式)____________。
(6)参照异戊二烯的上述合成路线,设计一条由A和乙醛为起始原料制备1,3-丁二烯的合成路线。
聚己二酸丙二醇酯是性能很好的耐热性和耐久性增塑剂。其中一种合成路线如下:
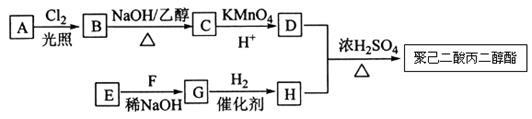
已知:①烃A的相对分子质量为84,核磁共振氢谱显示只有一种化学环境的氢;
②化合物B为一氯代烃;
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质;
④ 。
。
回答下列问题:
(1)A的结构简式为 。
(2)由B生成C的化学方程式为 。
(3)由E和F生成G的反应类型为 ,G的化学名称为 。
(4)①由D和H生成聚已二酸丙二醇酯的化学方程式为 。
②若聚已二酸丙二醇酯平均相对分子质量为5600,则其平均聚合度约为 (填标号)
a.30 b.35 c.40 d.48
(5)D的同分异构体中能同时满足下列条件的共有 种(不含立体异构):
①能与饱和NaHCO3溶液反应产生气体②既能发生银镜反应,又能发生水解反应。其中核磁共振氢谱显示为4组峰,且峰面积比为6:1:1:2的是 (写出其中一种结构简式)。
(6)请设计以甲苯、乙醛为有机原料(其他无机原料任选)合成肉桂酸(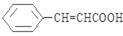 )的合成路线示意图。
)的合成路线示意图。
已知: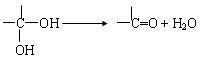
示例:
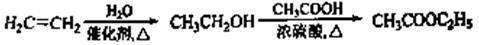
维拉佐酮是临床上使用广泛的抗抑郁药,其关键中间体合成路线如下: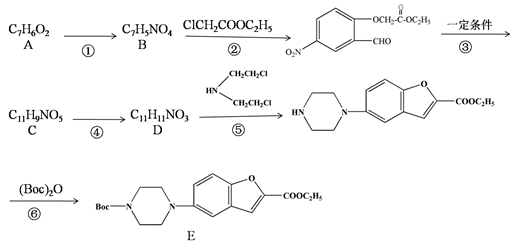
已知:
回答下列问题:
(1)反应类型:①________________④________________
(2)A和D的结构简式分别为:________________;________________
(3)写出反应②的化学方程式:_________________。实验中反应②在K2CO3弱碱性条件下进行的原因是:____________。
(4)同样具有三个支链,且支链结构与B完全相同,属于芳香族化合物的B的同分异构体一共有________种(不包括B)
(5)反应⑥中(Boc)2O是由两分子羧酸C5H10O3脱水形成的酸酐,且(Boc)2O分子中氢原子化学环境只有1种,写出(Boc)2O的结构简式:
(6) 实验室还可用 和
和  直接反应生成E,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式________。
直接反应生成E,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式________。
一定量的某有机物完全燃烧后,将燃烧产物通过足量的石灰水,经过滤可得沉淀10克,但称量滤液时其质量只减少2.9克,则此有机物不可能是( )
| A.乙二醇 | B.乙烯 | C.乙醇 | D.乙烷 |
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置进行了有关实验:

(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请直接在原图上把导管补充完整。
(2)实验中他们取6.4g铜片和12mL 18mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①请写出铜跟浓硫酸反应的化学方程式: ②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是: 。
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是:________(填写字母编号)。
A.铁粉 B.氯化钡溶液 C.银粉 D.碳酸氢钠溶液
(3)为定量测定余酸的物质的量浓度,某位同学进行了如下设计:先测定铜与浓硫酸反应产生SO2的量,再计算余酸的物质的量浓度。他认为测定SO2的量的方法有多种,请问下列实验方案中可行的是__________(填写字母编号)。其中计算结果余酸物质的量浓度比实际偏高的是_______________(填写字母编号)
A.将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B.将装置A产生的气体缓缓通入足量用稀硫酸酸化的高锰酸钾溶液,再加入足量氯化钡溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(已折算成标准状况)
D.将装置A产生的气体缓缓通入足量氢氧化钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
E.将装置A产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀(已知:硝酸具有强氧化性)
若A项不可行,请写出改进的方法:___________________(若A项可行则该空写“不用改进”)
向含等物质的量两种溶质的甲溶液中逐渐加入乙物质,生成不溶物的量(Y)与加入物的量(X)之间的关系符合如图所示的是( )
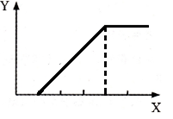
| |
甲溶液 |
乙物质 |
| A |
HCl和CaCl2 |
NaHCO3溶液 |
| B |
H2SO4和MgSO4 |
NaOH溶液 |
| C |
Fe2(SO4)3和CuSO4 |
Fe粉 |
| D |
AlCl3和HCl |
NH3气体 |
把20.95g干燥的氯酸钾与二氧化锰的混合物装入大试管中,加热到质量不变为止,剩余固体为16.15g,则:
(1)求生成的气体在标态下的体积
(2)剩余固体各成分的物质的量
(3)向剩余固体中加入过量的浓硫酸,全部氯元素成为两种含氯的混合气体,通入过量的碘化钾溶液,生成的碘被0.02mol Na2S2O3吸收,则生成的两种气体的体积(标态)是多少升?(已知:2Na2S2O3 +I2 → Na2S4O6+2NaI)
将26.8克KCl和KBr的混合物,溶于水配成500ml溶液,通入过量的Cl2,反应后将溶液蒸干,得固体22.35克。则原来所配溶液中K+、Cl-、Br-的物质的量之比为( )
| A.3︰1︰2 | B.1︰2︰3 | C.3︰2︰1 | D.1︰3︰2 |
中国海水资源丰富,回答下列问题:
(1)海水中主要含有 等离子(写离子符号,至少答出4种)。
(2)海水脱硫是一种有效除去火力发电产生的SO2的方法。其工艺流程如下图所示:

天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是: ;氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是 。
(3)下图是海水综合利用的一个方面。
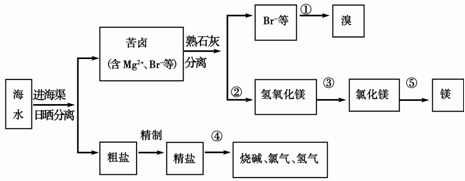
请回答下列问题:
I.①步主要反应的离子方程式: 。
溴及其化合物的用途有很多,写出其中的一种 。
II.第③步需要加入 ,其前面分离出氢氧化镁的操作称为 ,将镁条在二氧化碳中燃烧的产物为 。
III.粗盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤 正确的操作顺序是
利用硫酸厂烧渣(含铁的氧化物和少量FeS及SiO2)制碱式硫酸铁的流程如下:
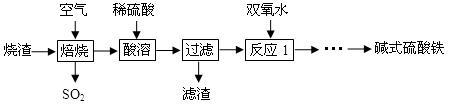
(1)SO2与过量NaOH溶液反应的离子方程式为 。
(2)滤渣的主要成分为 (填化学式)。
(3)反应1中加双氧水的目的是 。
(4)碱式硫酸铁的化学式为Fex(OH)y(SO4)z·nH2O,为确定其组成进行如下实验:
①称取1.6920 g 样品溶于足量的稀盐酸中;
②加足量的BaCl2溶液,过滤、洗涤、干燥、称重,得固体质量为2.3300 g;
③向步骤②的滤液中加过量的NaOH溶液,过滤、洗涤、灼烧、称重,得固体质量为0.6400 g。
根据以上实验数据计算碱式硫酸铁样品中的n(OH-): n(SO42-)(写出计算过程)
实验目的:为研究铁质材料与热浓硫酸的反应
(1)称取铁钉(碳素钢)12.0g放入30.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中是否含有Fe2+,应选择加入的试剂为 (选填序号)
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性KMnO4溶液
②乙同学取672 mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4然后加入足量BaCl2溶液,经适当操作后得到干燥固体4.66g。据此推知气体Y 中SO2的体积分数为 。
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
(2)气体Y中还有H2的原因是 。
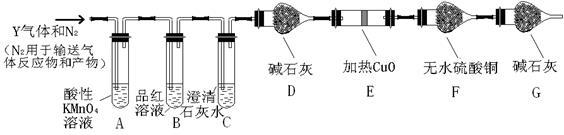
(3)装置A中试剂的作用是 ,反应的离子方程式 。
(4)简述确认气体Y中含有CO2的实验现象 。
(5)如果气体Y中含有H2,预计实验现象应是 。
试题篮
()