下列实验操作中错误的是( )。
| A.用规格为10 mL的量筒量取6m L的液体 |
| B.用药匙或者纸槽把粉末状药品送入试管的底部 |
| C.过滤时玻璃棒的末端应轻轻靠在三层的滤纸上 |
| D.如果没有试管夹,可以临时手持试管给固体或液体加热 |
分类是化学研究中常用的方法。下列分类方法中,不正确的是( )
①根据元素原子最外层电子数的多少将元素分为金属和非金属
②根据电解质在水溶液中能否完全电离将电解质分为强电解质和弱电解质
③依据组成元素的种类,将纯净物分为单质和化合物
④根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸等
⑤根据氧化物中是否含有金属元素,将氧化物分为碱性氧化物、酸性氧化物
⑥根据分散系的稳定性大小,将分散系分为胶体、浊液和溶液
⑦依据有无电子转移,将化学反应分为氧化还原反应和非氧化还原反应
⑧根据化学反应的热效应,将化学反应分为放热反应、吸热反应
| A.①④⑤⑥ | B.③④⑤⑥ | C.只有①③ | D.全部正确 |
蛭石为一种层状结构的含镁的铝硅酸盐,是黑云母等天然矿物风化蚀变的产物,因为其受热膨胀时呈挠曲状,形态酷似水蛭,故此得名蛭石。膨化后的蛭石呈颗粒状,有隔热、耐冻、抗菌、防火、吸声等优异性能,但不耐酸。
(1)某硅酸盐矿石的组成可以看作SiO2中有1/4的Si被Al置换,再由Mg平衡其电荷形成的。该矿石的组成以氧化物形式表示为 。
(2)某校研究性学习小组取得了某种牌号的膨化蛭石样品,其成分可以用氧化物(MgO、Fe2O3、Al2O3、SiO2、H2O)的形式表示。为研究蛭石的组成,拟进行实验探究,实验流程及相关数据如下: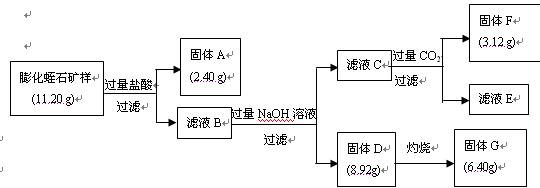
①固体A的化学式是 ;
②固体F的物质的量是 ;
③通过计算,给出用氧化物的形式表示某种膨化蛭石组成的化学式。
某合作学习小组讨论辨析:①将氯气通入氢氧化钠溶液可得到漂白液②可通过石油分馏得到甲烷、乙烯和苯③不锈钢和目前流通的硬币都是合金 ④硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 ⑤煤和石油都是可再生能源。上述说法正确的是
| A.①②④ | B.①③ | C.②③ | D.③⑤ |
“神州七号”三兄弟——LiH、LiD、LiT。其中Li的质量数为7,对这三种物质的下列说法正确的是 ( )
A. 质子数之比为1:2:3 B.中子数之比为1:1:1
质子数之比为1:2:3 B.中子数之比为1:1:1
C.摩尔质量之比为8:9:10 D.化学性质不相同
如图所示,在密闭容器中,一边装有一定量的金属钠,一边装有一定量的氧化汞,同时加热容器的两部分,钠和氧化汞都完全反应后,恢复到原温度,容器内空气 的成分仍不变。则钠和氧化汞的物质的量之比是( )
的成分仍不变。则钠和氧化汞的物质的量之比是( )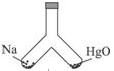
| A.1:1 | B.2∶1 | C.23∶216.6 | D.216.6∶23 |
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如右图转化关系(部分生成物和反应条件略去)。下列推断不正确的是 ( )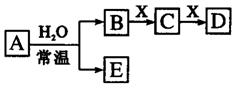
A.若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
B.若A 是单质,B和D的反应是
是单质,B和D的反应是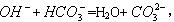 则E一定能还原Fe2O3C.若D为CO,C能和E反应,则A一定为Na2O2,其电子式是
则E一定能还原Fe2O3C.若D为CO,C能和E反应,则A一定为Na2O2,其电子式是
 D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
如下图带漏斗U型管中装有足量的煤油和水的混合物,静置后投入一小块碱金属。可观察到金属在煤油和水的界面a附近上下往复运动,下列说法不正确的是 ( )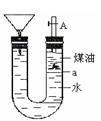
| A.此碱金属可能是钾或钠 |
| B.反应一段时间煤油会燃烧 |
| C.碱金属上下运动是由于与水反应产生了氢气 |
| D.若是金属锂则不能观察到上述现象 |
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示。若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是
| A.X的气态氢化物的水溶液显酸性 |
| B.X的原子半径小于Y |
| C.Z的最外层电子数比Y多 |
| D.W的非金属性比Z强 |
向100 mL 0.l mol·L—1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.l mol·L-1Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如右图所示。下列说法中正确的 ( )
| A.a点的溶液呈中性 |
| B.b点发生反应的离子方程式是:Al3++2SO2-4+2Ba2++3OH—→Al(OH)3↓+2BaSO4↓ |
| C.c点加入Ba(OH)2溶液的体积为200 mL |
| D.c点溶液呈碱性 |
重晶石矿的主要成分为硫酸钡,纯净的硫酸钡才能供医用作“钡餐”,在对某些内脏器官进行X 射线透视时服用。硫化钡是可溶于水的盐。讨论用重晶石矿制硫酸钡,设计流程如下: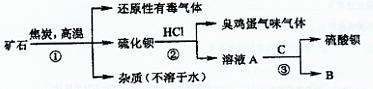
(1)写出步骤①的化学反应方程式 ,该反应产生的气体具有 、 等用途。
(2)为进行②反应先要分离出硫化钡溶液,采用的方法是 。在此之前要在溶液中滴入少量Ba (OH)2溶液,其作用是 。
(3)若B物质在该生产过程中可循环使用,则③反应的化学方程式是: 。
(4)有人提出②反应产生了有臭有毒的气体,可采用改变反应物的方法使无该气体产生,则②反应的化学方程式是: 。
此时若要B物质还能循环使用,则C为 (写化学式)。
(5) BaSO4是因为具有 、 等性质而可用作“钡餐”的。
下列叙述正确的是
| A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 |
| B.没有单质参加的反应一定不是氧化还原反应 |
| C.置换反应一定是氧化还原反应 |
| D.失电子难的原子,容易获得电子 |
试题篮
()