"加氢几分钟,畅行数百里",这是2021上海车展上为氢能源汽车打出的标语。氢能源汽车使用的是氢燃料电池(如图所示)。电池工作时在催化剂的作用下,氢原子失去电子形成氢离子,穿过电极A通过电解液移动到电极B与氧离子结合形成水分子;而电子则从电极A经外部电路通过电动机  到达电极B,形成电流。
到达电极B,形成电流。
(1)氢燃料电池工作时是将化学能直接转化为 能。
(2)氢气是氢燃料电池的原料,可以在用电低谷时,利用电网多余电能电解水来制取。已知1.2kg氢气大约可供某款氢能源汽车行驶100km,请根据化学方程式计算,制取1.2kg氢气至少需要电解多少质量的水。
(3)氢燃料电池工作时,通过电动机的电流方向是: 。
(4)世界能源组织提出:在制氢过程中基本上没有碳排放而得倒的氢气称为绿氢。下列方式可制得绿氢的是 。
| A. |
水力发电制氢 |
| B. |
太阳能发电制氢 |
| C. |
火力发电制氢 |
| D. |
核能发电制氢 |

天然气(主要成分为CH4)作为清洁能源,正逐步走进城乡居民生活。
(1)“西气东输”工程利于国家能源和产业结构调整,极大改善了沿线居民生活质量。
①为防止传输天然气的钢管被腐蚀,可采取的措施有 (写出一种)。
②CH4完全燃烧的化学方程式是 ,该过程 (填“释放”或“吸收”)能量。
③天然气的使用可有效减少酸雨形成。下列现象与酸雨有关的是 。
A.石刻文物被腐蚀
B.全球海平面上升
(2)工业上以CH4为原料生产H2,制取原理如图所示:

已知变换塔、洗涤塔发生的主要反应依次是:CO+H2O CO2+H2,CO2+H2O═H2CO3。
CO2+H2,CO2+H2O═H2CO3。
①“转化炉”中有H2产生,参加反应的CH4与H2O的质量比 = 。
= 。
②“洗涤塔”中气体从塔底通入,水从塔顶喷淋。这样操作的优点是 。
③若有32g CH4参与反应(假设各步反应都完全转化),理论上可制得 g H2。
(3)我国是世界上首个成功试采海域可燃冰的国家。可燃冰是CH4被H2O分子形成的笼包裹,在海底低温和高压作用下形成的结晶物质。
①可燃冰样品常存放于液氮储存罐中,其原因是 。
②可燃冰有多种结构,某H型可燃冰的化学式为CH4•9H2O,分析其结构发现:平均34个H2O分子构成6个笼,每个笼只容纳一个CH4或H2O分子。这6个笼内容纳的CH4与H2O分子个数比是 (填最小整数比)。

铅蓄电池在生产、生活中使用广泛。其构造示意图如图1,回答下列问题:

(1)铅蓄电池充电时是将电能转化为 (填序号)。
a、机械能 b、热能 c、化学能
(2)铅蓄电池放电过程中,反应的化学方程式为Pb+PbO 2+2H 2SO 4═2PbSO 4+2H 2O,据此可知,铅蓄电池在放电时,溶液的pH不断 (填"增大"、"减小"或"不变")。
(3)如图2是回收废铅蓄电池的一种工艺流程:
①从材料分类角度看,塑料是一类 材料。
②废硫酸可以与氟磷灰石[Ca 5(PO 4) 3F]反应,反应的化学方程式为2Ca 5(PO 4) 3F+7H 2SO 4═3CaSO 4+3Ca(H 2PO 4) 2+2HF,反应产物中可用作化肥的物质是 。
③如表是一些金属熔点的数据:
| 金属 |
锡 |
铅 |
铋 |
镉 |
| 熔点∕℃ |
231.9 |
327.5 |
271.3 |
320.9 |
日常所用保险丝由铋、铅、锡、镉等金属组成,其熔点约为 (填序号)
A.300﹣320℃
B.230﹣250℃
C.60﹣80℃
D.20﹣40℃
④废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
| 物质 |
CaCO 3 |
Ca(OH) 2 |
NH 3 |
NaOH |
| 市场参考价(元/kg ) |
1.8 |
2.0 |
6.5 |
11.5 |
已知:2NH 3+H 2SO 4═(NH 4)SO 4,如果要求花最少的钱来中和等质量、等浓度的废硫酸,则应选择 (填序号)。
a、CaCO 3 b、Ca(OH) 2c、NH 3d、NaOH。
小敏研究影响锌与盐酸反应快慢的因素。
| 序号 |
盐酸溶液浓度 |
2分钟内产生氢气的体积 |
| 1 |
5% |
10mL |
| 2 |
15% |
28mL |
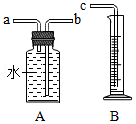
(1)图甲中A、B仪器可以组装一套测量气体体积的装置,利用该装置时A中的 管接c。
(2)他选用2克完全相同的锌片分别和同体积5%、15%的稀盐酸进行实验。获得表格数据。由此推断实验是通过 来体现反应快慢的。
(3)小敏分析数据得到如下结论:锌与盐酸反应快慢与盐酸浓度有关,盐酸浓度越大反应越快。其他同学认为结论不可靠,他们的依据是: 。
(4)实验中小敏发现锌与盐酸反应时,一开始产生氢气速度并没有随盐酸浓度的减少而减慢,查阅资料得知化学反应中往往伴随着能量变化。由此作出猜想:锌与盐酸反应快慢还与 有关。
同学们利用如图所示的装置,对质量守恒定律进行了探究。实验结束后,老师另外提出了几个问题,请你一起参与思考。
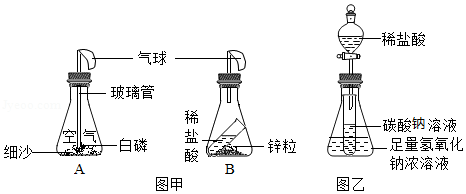
(1)图甲装置内物质充分反应后,冷却至室温,气球仍胀大的是 (选填“A”、“B”或“A和B”)
(2)若图乙装置内Na2CO3溶液的质量为5克,滴入试管的稀盐酸质量也是5克,装置内物质充分反应后,发现NaOH浓溶液质量增加0.22克,试管中滴入紫色石蕊试液变红。根据上述已知条件,通过分析可以确定的是 (选填序号)
①原稀盐酸的溶质质量分数 ②原Na2CO3溶液的溶质质量分数
③原NaOH溶液的溶质质量分数 ④反应后试管中NaCl的溶质质量分数
请你选择所填的其中一项,通过计算确定其溶质质量分数是多少?
试题篮
()