(1)已知:难溶电解质Cu(OH)2在常温下的KSP=2×10-20,则常温下:
①某CuSO4溶液中c(Cu2+)=0.02mol∙L-1,如要生成Cu(OH)2沉淀,应调整溶液的pH最小为_____________。
②要使0.2mol∙L-1 CuSO4溶液中的Cu2+沉淀后,使溶液中Cu2+的浓度为2×10-6mol∙L-1,则应向溶液里加入NaOH溶液,使溶液的pH为______________。
(2)将0.2mol∙L-1HA溶液与0.2mol∙L-1NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-),则(用“>”、“<”或“=”填写下列空白)。
①混合溶液中,由水电离出的c(OH-)__________0.2mol∙L-1HA溶液由水电离出的c(H+);
②25℃时,如果取0.2mol∙L-1HA溶液与0.11mol∙L-1NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度_________NaA的水解程度。
某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还含有一定量的SiO2)可用于制备FeCO3,其流程如下: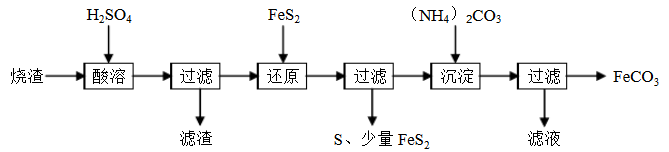
已知:还原时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、II被还原,其中反应Ⅰ为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+。
(1)反应Ⅰ中还原剂是___________________。
(2)滤渣的成分是___________(填名称)。
(3)所得FeCO3需充分洗涤,检验FeCO3是否洗净的方法是__________________。
(4)①配平反应II的离子方程式:_______Fe3++_______FeS2=_______S↓+_______Fe2+。
②还原前后溶液中部分离子的浓度见下表(溶液体积变化忽略不计):
| 离子 |
离子浓度(mol∙L-1) |
|
| 还原前 |
还原后 |
|
| Fe2+ |
0.10 |
2.50 |
| SO42- |
3.50 |
3.70 |
则反应Ⅰ、II中生成Fe2+的物质的量之比为_________。
现有一定量铝粉和铁粉的混合物与一定体积稀硝酸充分反应,反应过程中无气体放出(硝酸的还原产物是NH4NO3)。在反应结束后的溶液中,逐滴加入2mol∙L-1的NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量的关系如图所示。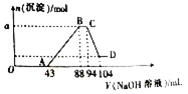
(1)写出OA段反应的离子方程式:____________________________。
(2)B点时溶液中含有溶质的化学式为____________。
(3)a的数值为__________。
(4)原硝酸溶液中HNO3的物质的量为__________mol。
在某澄清溶液中,可能存在下列几种离子:H+、K+、Ba2+、SO42-、I-、CO32-。取该溶液进行下列实验:①用pH试纸检验,该溶液呈强酸性;②取200mL溶液加入少量氯水和少量CCl4,振荡后静置,CCl4层呈紫色;③另取部分溶液逐滴加入NaOH溶液,当溶液呈碱性时,再加入Na2CO3溶液,有白色沉淀生成。
(1)根据上述实验现象,推断原溶液中肯定存在的离子是_____________,肯定不存在的离子是_______,可能存在的离子是____________。
(2)若步骤②中消耗0.1molCl2,则溶液中与Cl2反应的离子的物质的量浓度为________________。
(3)写出实验③中生成白色沉淀的离子方程式:____________________。
掺杂微量铜、硼、镓、硒等元素的单晶硅太阳能电池是第三代太阳能电池之一。
(1)Cu2+的电子排布式为___________________。
(2)已知铜转化为水合离子过程如下:
已知I1=745.5kJ/mol,I2=1957.3kJ/mol。在水溶液中Cu2+比Cu更稳定的原因是_____________。
(3)铜与类卤素(SCN)2反应生成Cu(SCN)2。1mol(SCN)2含有π键的数目为_______________。HSCN有两种结构,H-S-C≡N(硫氰酸)的沸点低于H-N=C=S(异硫氰酸)的沸点,其原因是_________________。
(4)BF3能与NH3反应生成配合物BF3-NH3,该配合物中B原子的杂化方式为___________________。
(5)铜和硒可形成的半导体团簇分子的球棍模型如图所示,其分子式为__________________。
(6)镓与某有机物形成的配合物过程如下图,在图上画出产物中的配位键。
(7)与Si同周期部分元素的电离能如下图所示,其中a、b和c分别代表_____________。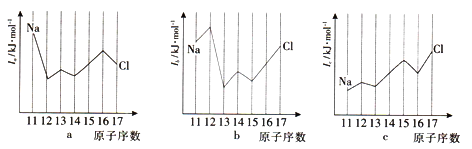
| A.a为I1、b为I2、c为I3 | B.a为I2、b为I3、c为I1 |
| C.a为I3、b为I2、c为I1 | D.a为I1、b为I3、c为I2 |
利用废旧镀锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO,制备流程图如下:
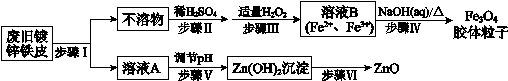
已知:Zn及其化合物的性质与Al及其化合物的性质相似。
回答下列问题:
(1)步骤I中所用的试剂是___________。
(2)步骤III中反应的离子方程式是__________________________________。
(3)步骤V可选用的试剂是_________(填序号)。
a.NaOH溶液 b.氨水 c.盐酸
(4)步骤VI的实验操作是_____________。
处理SO2废气的一种工艺流程如下图所示:
O2是氧化剂;(2)根据(1)的分析,得出:
根据流程,回答下列问题:
(1)溶液B与空气发生反应生成溶液C,其中氧化剂是________。
(2)SO2和酸性Fe2(SO4)3溶液反应的离子方程式是____________________________。
(3)推断Fe3+、O2和SO42−的氧化性由强到弱的顺序是_________________________。
过氧化钙(CaO2)是一种白色、无毒、难溶于水的固体,能杀菌消毒,广泛用于果蔬保鲜、空气净化、污水处理等方面。
(1)CaO2溶于盐酸可得H2O2,反应的化学方程式是 。
(2)CaO2在保存时要密封,避免接触水蒸气和二氧化碳。水蒸气与CaO2反应的化学方程式是 。
(3)已知:CaO2在350℃迅速分解生成CaO和O2。取某CaO2样品10 g(含有少量CaO杂质),充分加热后剩余固体的质量为8.4 g,则该样品中CaO2的质量分数为 。
现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
已知反应I为:NaCl + CO2 + NH3 + H2O === NaHCO3↓+ NH4Cl
(1)工业生产中,制备NH3的化学方程式是_____________________________。
(2)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO42−等离子。
① 为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中___________________________,过滤;
c.向滤液中___________________________,过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
② 步骤c中反应的离子方程式是______________________________。
(3)反应II的化学方程式是_________________________________。
(4)制得的纯碱中含有少量NaCl。取5.5 g纯碱样品加入足量稀硫酸,得到标准状况下1120 mL CO2。则样品中纯碱的质量分数是_________%(保留1位小数)。
从铝土矿(主要成分是Al2O3,含Fe2O3、MgO和一些不溶于酸碱的杂质)中提取氧化铝两种工艺流程如下:

请回答下列问题:
(1)写出步骤②中加入烧碱后的离子方程式为_________________ _____________。
(2)列举氧化铝的两种常见的用途____ ______、________ __________。
(3)沉淀C的主要成分是______________ ______________(填化学式)。滤液D与少量CO2反应的离子方程式为___________ ________________。
(4)步骤③、④中不能用硫酸代替CO2,原因是__________________ _____________。向该滤液M中加入少量澄清石灰水的离子方程式为____________ ______________。
(5)沉淀F在过滤后需要洗涤,请写出检验F是否洗涤干净的方法_________ ________。
(6)若现在有10t的铝土矿,其中铝元素的质量分数为10.8%,则在流程乙中溶解时,需要4mol/L的NaOH溶液至少_____ __L。
仔细观察下图,根据题意对图中两极进行必要的连接后填空:
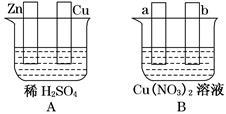
(1)若在图A中,使铜片上冒H2气泡。则加以必要的连接后的装置叫 。
(2)若在图B中,a、b为惰性电极,进行必要的连接后使b极析出1.28g铜,则a极析出的物质的物质的量为 ,反应的总反应方程式为 。
(3)若将图A中Zn、Cu两极与图B中a、b作必要的边接后,也能产生与(1)、(2)完全相同的现象,则Cu极连_______极(填a或b)。经过一段时间后,停止反应并搅匀溶液,图B中溶液的pH_________(填写“升高”、“降低”或“不变”),欲使溶液恢复至与反应前完全一致,则应加入的一定量的物质是_________。
| A.CuO | B.Cu(OH)2 | C.Cu2(OH)2CO3 | D.CuCO3 |
室温下,某同学将某一元酸HX和NaOH溶液等体积混合,测得两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 |
HX物质的量 浓度(mol/L) |
NaOH物质的 量浓度(mol/L) |
混合溶液的pH |
| 甲 |
0.2 |
0.2 |
pH=a |
| 乙 |
c1 |
0.2 |
pH=7 |
| 丙 |
0.2 |
0.1 |
pH>7 |
| 丁 |
c2 |
c2 |
pH=10 |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,若HX为强酸,则a 7(填“>”“<”或“=”);若HX为弱酸,则a 7(填“>”“<”或“=”)。
(2)在乙组混合溶液中离子浓度c(X-)与c(Na+)的大小关系是 。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HX是 酸(填“强”或“弱”),该混合溶液中离子浓度由大到小的顺序是 。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)= mol/L。
在恒容的密闭容器中,进行化学反应CO2 (g)+H2 (g) CO (g)+H2O (g),其化学平衡常数K和温度t的关系如下表:
CO (g)+H2O (g),其化学平衡常数K和温度t的关系如下表:
| t / ℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=____________。
(2)正反应为________反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是________(多选无分)。
A.容器中压强不变 B.混合气体中c (CO)不变
C.v正(H2)=v逆(H2O) D.c (CO2)="c" (CO)
(4)某温度下,平衡浓度符合下式:c (CO2)·c (H2)="c" (CO)·c (H2O)。可判断此时的温度为________℃。
| 实验 编号 |
HX物质的量 浓度(mol/L) |
NaOH物质的 量浓度(mol/L) |
混合溶液的pH |
| 甲 |
0.2 |
0.2 |
pH=a |
| 乙 |
c1 |
0.2 |
pH=7 |
| 丙 |
0.2 |
0.1 |
pH>7 |
| 丁 |
c2 |
c2 |
pH=10 |
某待测液中可能含有Ag+、Fe3+、K+、Ba2+、NH4+ 5种离子,现进行如下实验:
(1)加入过量的稀盐酸,有白色沉淀生成。
(2)过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
(3)过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现。
(4)另取少量步骤(3)中的滤液,加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:待测液中一定含有的离子是 ,一定不含的离子是__________,还有一种离子不能确定是否存在,要检验这种离子的实验方法是 。
洪灾过后,需要对饮用水进行杀菌消毒,防止传染性疾病的爆发。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为 ;
(2)实验室常用软锰矿(主要成分为MnO2)和浓盐酸反应制Cl2,其化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,其中,氧化产物是 (填化学式),在每摩尔参加反应的盐酸中,作还原剂的盐酸的物质的量为 mol。
MnCl2+Cl2↑+2H2O,其中,氧化产物是 (填化学式),在每摩尔参加反应的盐酸中,作还原剂的盐酸的物质的量为 mol。
试题篮
()